Modern fiziğin tanımına göre proton, maddeyi oluşturan atom altı parçacıklardan birisi olarak kabul edilmektedir. Pozitif bir elektrik yüke sahip olarak tanımlanan protonun, farklı elementlerde farklı sayıda olması nedeniyle de elementlerin niçin birbirinden farklı olduğunu açıklar.
Protonun yanı sıra, atomu oluşturan diğer iki parçacık daha bulunmaktadır. Bu parçacıklar nötron ve elektron olarak bilinir. Nötron ve proton, güçlü nükleer kuvvet sayesinde atomun çekirdeği içinde adeta birbirlerine sıkı sıkıya bağlı bir şekilde durur.
Elektron ise çok genel bir tabirle proton ve nötronun oluşturduğu çekirdek etrafında “dolanmaktadır”. Ancak elektronun hareketi, dolanmak kelimesiyle aklımıza gelen “etrafında dönmek” olgusuyla tam olarak aynı şey değildir.
Çünkü fizikçiler, elektronun atom çekirdeği etrafındaki davranışını birtakım kuantum fiziksel etkilerle açıklıyor. Ya da daha doğru bir ifadeyle elektronun kendine has doğası o şekilde olduğu için fizikçiler de elektronun hareketini kuantum fiziğine başvurarak modellemeye çalışıyorlar.
Elektron, günlük yaşantımızda karşılaştığımız olguların tamamen dışında bir şekilde, adeta olasılıklar halinde atom çekirdeği etrafında bulunur.
Bir diğer ifadeyle elektron, çekirdeğin etrafında bir konumda ve sabit bir hızda değil, ancak her bir konumdaki varlığı belli olasılıklara dayanacak şekilde mevcuttur.
Kolay anlaşılması adına şunu söyleyebiliriz ki adeta çekirdeğin çevresinde bir elektron alanı var ve kimi zaman elektron bir dalga gibi kimi zaman da bir parçacık gibi davranıyor. Hatta daha doğru ifadeyle elektron, ne dalga gibi ne de parçacık gibi davranmaktadır. Elektronun davranışı, günümüzde sadece matematiksel denklemlerle açıklanabiliyor.
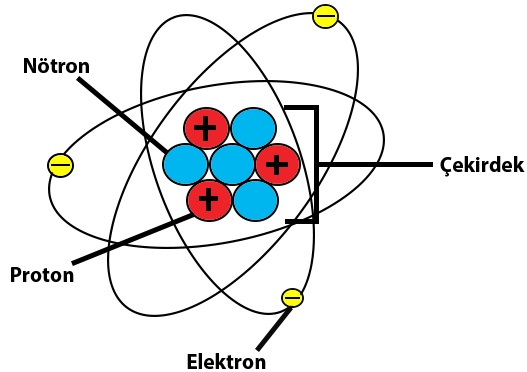
Görüldüğü üzere elektronun doğası, günlük hayattaki sağduyumuzla alışık olduğumuz olgulardan tamamen farklı bir şekilde davranıyor. Bu yüzdendir ki doğru bir atom modelinin oluşturulması için fizikçiler neredeyse bir yüzyıl boyunca atomun doğasının nasıl olduğuyla ilgili çeşitli modeller ortaya atmıştı.
Konumuza geri dönecek olursak proton ve nötronun birlikte atomun kütlesinin %99.9’undan sorumlu olduğunu ifade edebiliriz. Nötron ile kütlesi neredeyse aynı olan proton, elektrondan yaklaşık 1840 kat daha ağır bir atom altı parçacıktır.
Her atomun çekirdeğinde en az bir tane olmak üzere çeşitli sayıda proton bulunmaktadır. Yazının başında da belirttiğimiz gibi atom çekirdeğindeki proton sayısı, elementin karakterini belirleyen yegane unsurdur.
Örneğin hidrojen atomunun çekirdeğinde sadece 1 proton bulunmaktadır. Dolayısıyla bu elemente hidrojen elementi ismini veririz. Öte yandan karbon atomu, 6 protona (ve 6 nötrona) sahiptir. Bu yüzden de karbon atomu özelliğini taşır.
Görüldüğü gibi elementleri oluşturan atomlar farklı sayıda proton içerdikleri için elementler de birbirlerinden farklılık gösterir.
Buraya kadar protonun ne olduğundan, atomun yapısındaki yerinden ve özelliklerinden kısaca bahsettik. Peki atomu oluşturan temel parçacıklardan biri olan proton nasıl keşfedilmişti? Bu kadar küçük bir yapıda olmasına rağmen bilim insanları protonu nasıl tespit edebildi ki?
Hidrojen Çekirdeği Olarak Protiller
Ernest Rutherford tarafından atomun bir çekirdeğe sahip olduğu keşfedilmeden önce, atomların hidrojen çekirdeğinden oluştuğu şeklinde bilim camiasında genel bir inanış mevcuttu.
Bu inanışı ise tek bir kişiye atfetmek doğru olmaz. Çünkü atomların temel yapısında aslında hidrojenin var olduğu kanısı uzun yıllar boyunca bilim insanları tarafından kabul edilen bir görüştü.
Örneğin 1815 gibi bir tarihte William Prout, bütün atomların hidrojenden, kendi ifadesiyle “protillerden” meydana geldiğini öne sürüyordu.
Prout’un ortaya attığı bu görüş, Prout Hipotezi olarak bilinmektedir. Hipoteze göre hidrojen atomu, var olan tek tür parçacıktı ve geri kalan elementler de farklı sayıdaki hidrojen atomlarından oluşmaktaydı.
Elektron Keşfediliyor
Protonun keşfedilmesinden önce daha kat edilecek uzun bir yol vardı. Örneğin elektronun keşfedilmesi. Bu noktada elektronun, protondan neden daha önce keşfedildiği sorusu gündeme gelebilir.
Çünkü proton, atomun çekirdeğini oluşturan iki temel parçacıktan bir tanesidir. Protonun keşfedilmesi için öncelikle atomun bir çekirdeğe sahip olduğunun anlaşılması gerekecekti. Çekirdek ise atoma göre oldukça küçük bir yapıdaydı.
Elektron ise protondan daha dışta ve tespit edilmesi daha kolay bir parçacık olduğu için onun keşfedilmesi de tarihte daha önce gerçekleşmiştir diyebiliriz.
Elektron, katot ışın tüpleri denilen bilimsel bir alet kullanılarak keşfedilmişti. Bilim insanlarının yaptığı bu deney, en basit haliyle şöyledir:
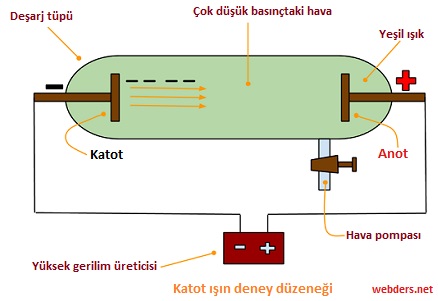
Deneyde bir katot ışın tüpü vardır ve bu tüpün içi neredeyse havadan tamamen arındırılmış olarak boş bir haldedir. Tüpün iki ucuna ise pozitif ve negatif yüklü olmak üzere iki elektrot yerleştirilir.
Sonrasında negatif elektrottan pozitif olanına doğru olacak şekilde bir elektrik akımı gönderilir. İlginç bir şekilde bu işlem yapılırken tüpün içinde birde ışın demeti ortaya çıkıyordu.
Yapılan bu işlemlerin sonucunda bilim insanları, ortaya çıkan ışın demetlerinin akış yönünü gözlemleyerek ışınları oluşturan parçacıkların negatif bir yüke sahip olduğu çıkarımını yapmıştı. Bu parçacıklar aslında elektrondu.
Elektron keşfedildi keşfedilmesine ama bu deneylerin sonucunda temel bir soru gün yüzüne çıkmaktaydı. Eğer katot ışınları, katotun atomlarından ayrılan negatif yüklü elektronlarsa, bu elektronları kaybeden atomlardan geriye ne kalıyordu?
Bu noktada şu bilgiyi vermekte fayda var. Atomlar bilindiği kadarıyla hiçbir elektrik yüküne sahip değildir. Bu şu anlama geliyor: Her atom tam olarak aynı sayıda pozitif ve negatif yüklü parçacık içermelidir.
Bir hidrojen atomu ise, sadece bir elektrona sahip olan en basit atom çeşidi olduğuna göre, eğer elektron bir atomdan ayrılırsa o halde geride pozitif yüklü bir parçacık kalmalıdır.
Atomun Bir Çekirdeğe Sahip Olduğunun Keşfedilmesiyle Yeni Bir Atom Modeli Ortaya Çıkıyor
Yeni Zelandalı fizikçi Ernest Rutherford, 1911 yılında gerçekleştirdiği ünlü “altın folyo deneyi” ile tarihte atomun çekirdeğini deneysel olarak keşfeden ilk bilim insanı unvanına layık kişi olmuştur.
Yaptığı altın folyo deneyinde Rutherford, son derece ince bir altın folyo tabakayı, alfa parçacıkları ışınıyla adeta bombardımana tutmuştu.
Yeni Zelandalı fizikçi, başlangıçta hiçbir şey fark etmedi. Bunun üzerine öğrencilerine, deneyi tekrar yapıp bir süre boyunca gözlemlemelerini istiyordu.
Bir hafta, iki hafta, üç hafta geçiyor ancak öğrenciler herhangi bir şey tespit edemiyordu. Nihayet birkaç haftanın sonunda, alfa parçacıklarının çok küçük bir kısmının folyodan sekip saçıldığını gözlemlediler.
Çok daha az bir kısmının, yani yaklaşık her 8000 alfa parçacığının sadece 1 tanesinin ise geldiği yöne doğru geri sektiğini gören öğrenciler Rutherford’a bu gözlemi bildirmeleri üzerine Rutherford, bu deneyin sonucunda atomun merkezinde bir çekirdeğin var olduğu görüşünü savunmuştu.
Peki bu ne anlama geliyordu? Alfa parçacıkları pozitif yüke sahip olduğu ve belirli bir sapma gösterdiği için Rutherford, bir atomun içindeki bütün pozitif yüklü parçacıkların atomun çekirdeğinde bulunduğu çıkarımını yaptı.
Alfa parçacıklarının çok küçük bir kısmının saptığı gerçeğinden de yola çıkan Rutherford, atomun çekirdeğinin çok küçük, öyle ki atomun kendisinden yüzlerce kat küçük olduğu sonucunu rahatlıkla görebilirdi.
Böylelikle Rutherford, yeni bir atom modeli ortaya atmak üzereydi. Rutherford Atom Modeli olarak da bilinen bu modele göre atom, çoğunlukla boşluktan ibaretti. Merkezindeki çekirdek ise çok küçük bir hacmi kaplıyordu.
Elektronlar, bu atom çekirdeğinin etrafında dönmekteydi. Ayrıca Yeni Zelandalı fizikçi, çekirdekteki pozitif yüklü parçacıkların toplam sayısının, etrafındaki elektronların sayısına eşit olduğunu da söylüyordu.

Proton Keşfediliyor – Tarihteki İlk Simyacı Ernest Rutherford
İnsanlık, doğa bilimleriyle ilk uğraştığı dönemlerden beri bir elementi başka bir elemente çevirebilmek amacıyla türlü deneylere başvurmuştu.
Hatta Isaac Newton gibi büyük bir dahi bile elementleri altına dönüştürme gibi bir işe hayatının önemli bir kısmını adamıştı.
Her ne kadar aynı niyetle olmasa da tarihte bir elementi başka bir elemente ilk defa dönüştüren kişinin Ernest Rutherford olduğunu söyleyebiliriz. Nasıl mı?
Marie Curie’nin 20.yüzyılın başında radyoaktif özelliğe sahip radyum elementini keşfetmesinden sonra Rutherford, bu elementle alakalı deneyler yapmaya başlamıştı.
Deney esnasında radyumu, içi hava dolu bir cam tüpe koymuştu. Rutherford bunun üzerine kullandığı detektörle bir şey fark etti. Hidrojen çekirdeği olarak bilinen bir alfa parçacığı ışıması, hiçlikten ortaya çıkıvermişti.

Deneyi daha da derinleştiren Yeni Zelandalı fizikçi, havayı meydana getiren nitrojen, oksijen gibi elementler ile aynı deneyi tekrardan yapmaya karar verdi.
İçi nitrojen dolu tüpün içindeki radyumun varlığı nedeniyle nitrojenin iki farklı elemente, oksijen ve hidrojene dönüştüğünü gözlemlemişti.
Buradan sadece bir sonuç çıkabilirdi: Hidrojen çekirdeği, nitrojen atomunun varlığı sayesinde ortaya çıkıyordu. Bu da demek oluyordu ki hidrojen çekirdeği, bütün diğer atomların bir parçasıydı.
Ernest Rutherford, bir elementin başka bir elemente dönüşmesini sağlayarak tarihteki ilk simyacı olmuştu aslında. Nitrojen elementinden hidrojen çekirdeği meydana getirerek, binlerce yıldır insanlığın yapamadığı bir işi başarmıştı.
Rutherford 1920 yılında bu hidrojen çekirdeğinin yeni bir parçacık olduğunu öne sürdü. İsmini de proton koymuştu. Proton, Yunanca da “ilk” anlamına gelen “protos” kelimesinden gelmekteydi.
Sonuç:
Maddenin en temel yapıtaşlarından biri olan proton, 1920 yılında Ernest Rutherford tarafından keşfedilmiştir. Ancak atomun gizemli dünyasına ilişkin macera, burada sonlanmayacaktı.
Fizikçiler, protonun haricinde atomun çekirdeğini meydana getiren bir diğer parçacığı, herhangi bir yüke sahip olmayan nötronu da ilerleyen yıllarda keşfedecekti.
Ancak nötronun bile atom yapbozunda son parça olduğunu söyleyemeyiz. Bundan sonra fizik, öyle bir dönüşüm geçirecekti ki 20.yüzyıla kadar hakim olan fizik anlayışı, atomun gizemli ve bir o kadar da sağduyuya aykırı doğasını açıklamakta yetersiz kalacaktı.
Artık yepyeni bir fizik anlayışının ortaya çıkması gerekiyordu: O fizik anlayışı da Kuantum fiziğiydi. Niels Bohr ve Erwin Schrödinger gibi fiziğin dev isimlerinin başını çektiği bu yepyeni fizik anlayışı, gelecek yıllarda yapılacak olan keşiflerin gerçekleşmesini mümkün kılan nihai fizik modeli olacaktır.
Fakat kuantum fiziği ve devamında yapılan keşifler, başka yazıların konusu.